期刊發(fā)表
楊旗教授團隊在《Advanced Science》報道基于RGD多肽靶向的金屬有機骨架衍生的類卟啉結構介孔碳球納米材料介導的雙光療溶栓新應用
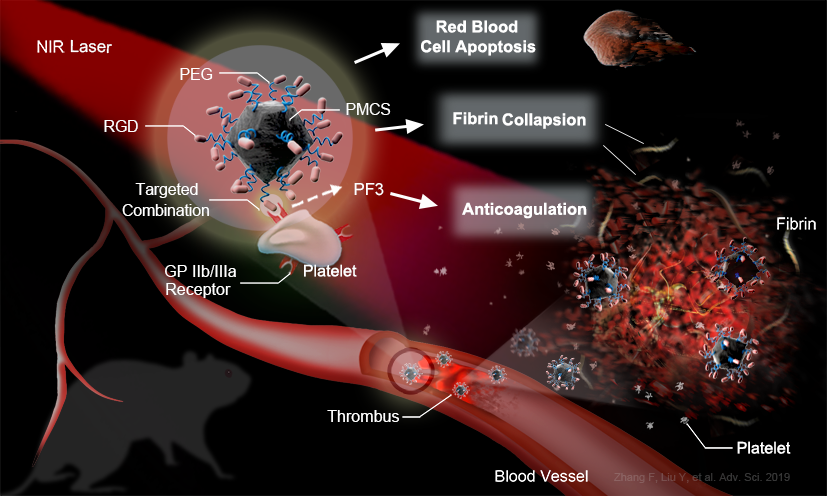
2019年7月,首都醫(yī)科大學宣武醫(yī)院放射科楊旗教授團隊與北京化工大學劉惠玉教授團隊合作在《Advanced Science》(2018 IF: 15.8)上發(fā)表題為“Metal–Organic‐Framework‐Derived Carbon Nanostructures for Site‐Specific Dual‐Modality Photothermal/Photodynamic Thrombus Therapy”(DOI: 10.1002/advs.201901378)的研究成果。該研究基于RGD肽對GPIIbIIIa整合素受體的靶向結合作用,偶聯(lián)金屬有機骨架衍生的類卟啉結構介孔碳球納米材料實現(xiàn)血栓的雙光療。楊旗教授與北京化工大學劉惠玉教授為共同通訊作者。

血栓相關疾病,如缺血性卒中,急性心肌梗死、深靜脈血栓形成等,有高致死率和致殘率。目前以纖維蛋白溶解藥物為代表的溶栓藥廣泛應用于臨床。但是該藥溶栓后致命的出血風險成為其現(xiàn)有臨床應用的一大局限。因此尋找更精準同時相對安全有效的溶栓方法對于降低溶栓出血風險,改善溶栓治療預后具有重要意義。研究表明,部分納米材料能在近紅外光照射下通過Landau阻尼效應使晶格震動加劇,將光能轉化為熱能并對材料鄰近分子蛋白結構產(chǎn)生破壞。本研究使用靶向納米試劑介導的雙模態(tài)近紅外光溶栓,著重提高生物安全性及溶栓效應。靜脈注射合成納米劑后,其可主動靶向結合血栓上的GPIIb/IIIa受體,通過近紅外光在血栓位點進行能量轉化,使纖維蛋白骨架結構及紅細胞等重要血栓組成成分崩解,從而實現(xiàn)有效溶栓。本研究中通過單次光療,使用7.0 T高場磁共振在體成像證實在下肢血栓模型中再通率達到87.9%。并且本研究還發(fā)現(xiàn)雙光療同時產(chǎn)生對血小板三因子的抑制,從而發(fā)揮潛在的抗原位血栓再形成的作用。綜合研究結果表明,該策略是一種無創(chuàng)、有效的溶栓方案。
近年來,精準醫(yī)療獲得迅猛發(fā)展。在心腦血管疾病診療領域,越來越多的醫(yī)生、專家對精準醫(yī)療達成共識。中國心腦血管病診療已邁入精準醫(yī)療時代。在精準醫(yī)學的潮流之中,該研究取得了心腦血管病精準治療的一大進步。其提出的創(chuàng)造性溶栓策略實現(xiàn)了對血栓的精準靶向治療,推進了納米技術在心血管疾病,特別是血栓相關疾病的新應用。其使用有望克服全身溶栓藥物的臨床局限。也為血栓相關心腦血管疾病的納米生物科學研究提供了新的技術和思路。一個從分子水平、從個體化角度認識、防控疾病的精準醫(yī)學時代正在穩(wěn)步發(fā)展。